ou
Orbitales et indétermination quantique
![]() L'atome
quantique
L'atome
quantique
Revenons à notre atome; la physique quantique va rendre le modèle de Bohr caduque et le remplacer par un modèle plus flou... plus difficile à se représenter.
 En
effet, nous avons vu que l'électron quantique est un agent double
victime de la dualité onde-corpuscule. L'onde associée à
l'électron correspond en fait à une probabilité de
trouver ledit électron quantique en un endroit donné.
En
effet, nous avons vu que l'électron quantique est un agent double
victime de la dualité onde-corpuscule. L'onde associée à
l'électron correspond en fait à une probabilité de
trouver ledit électron quantique en un endroit donné.
La particule n'est plus un point matériel classique mais un
paquet d'ondes probabilistes, une superposition de mouvements potentiels.
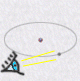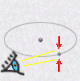
Les orbites électroniques doivent faire place à la notion
d'orbitales, sorte de sphères floues et probabilistes, dans
lesquelles l'électron serait en quelque sorte dilué tout
autour du noyau.
Ce n'est que lorsque les physiciens interagissent avec l'atome pour
observer l'électron, que ce dernier leur apparaît comme une
particule: C'est comme si le nuage électronique ondulatoire se réduisait
soudain en une particule bien matérielle. S'il fallait risquer une
image pour illustrer ce curieux phénomène, on pourrait imaginer
l'électron comme un sous-marin qui émerge, le temps d'une
mesure, de son océan probabiliste. Plus tard, il y replongera et
il sera impossible à un observateur de surface de le localiser avec
précison: on ne pourra plus que définir le volume de l'océan
où le sous-marin peut probablement se trouver.
| orbitale électronique | électron observé |
| nature ondulatoire | nature corpusculaire |
 |
 |
Ce nouveau modèle de nuages électroniques obéit
à un principe clé de la physique quantique: Le principe
d'indétermination d'Heisenberg.
Si nous étions réduit à l'échelle de
l'atome, que verrions-nous?
|
|
|
![]()
![]() Le
principe d'indétermination d'Heisenberg
Le
principe d'indétermination d'Heisenberg
 Outre
le fait que le physicien allemand Werner Heisenberg est le père
de cette loi (parfois aussi nommée principe d'incertitude),
que nous dit ce principe ? qu'il est impossible de déterminer avec
précision et simultanément la position et la vitesse d'une
particule comme l'électron. La notion de trajectoire exacte n'a
pas de sens pour les particules. Ce paradoxe quantique (encore un!) est
lié à la difficulté d'observer un électron...
Comment l'observer?
Outre
le fait que le physicien allemand Werner Heisenberg est le père
de cette loi (parfois aussi nommée principe d'incertitude),
que nous dit ce principe ? qu'il est impossible de déterminer avec
précision et simultanément la position et la vitesse d'une
particule comme l'électron. La notion de trajectoire exacte n'a
pas de sens pour les particules. Ce paradoxe quantique (encore un!) est
lié à la difficulté d'observer un électron...
Comment l'observer?
On ne peut observer quelque chose qu'en l'éclairant avec de la
lumière. Or à l'échelle de l'infiniment petit, cela
pose un problème tout à fait nouveau. Le moindre photon qui
percute ou interagit avec un électron va modifier la trajectoire
initiale de ce dernier ou le faire changer d'orbitale. A cette échelle,
le photon devient un projectile qui pourra déterminer la position
de l'électron, mais qui aura en même temps modifié
sa vitesse et sa trajectoire; celle ci ne pourra donc pas être connue
en même temps. La moindre mesure interfère avec l'objet de
la mesure. et la change!
![]() Pt'Hibou
le hibou quantique.
Pt'Hibou
le hibou quantique.
Osons une nouvelle image pour illustrer ce principe: La nuit au fond
des bois, un amoureux de la nature entend le hululement d'un hibou. S'il
veut, en même temps, voir le volatile, il devra braquer sur lui une
lampe torche: Il est à parier que le hibou, ébloui, arrêtera
son chant. D'où le dilemne insoluble: On ne peut pas à la
fois entendre et voir le hibou...Hélas!

![]()