La physique quantique 1
ou
Lumière sur le photon
![]() Introduction
Introduction
La théorie quantique est utilisée par les physiciens pour rendre compte des phénomènes qui ont cours à l'échelle microscopique des particules.
 La
puissance oprératoire de cette physique est considérable.
Elle est désormais utilisée par les physiciens nucléaires
et atomistes, par les physiciens du solide et même par les astrophysiciens.
A ce jour, aucune expérience n'est venue démentir ses prédictions,
aussi étranges soient-elles. La physique quantique utilisant des
concepts qui n'ont pas toujours de contrepartie dans la vie courante, il
ne faut pas s'étonner si certaines de ses prédictions heurtent
si violemment le sens commun.
La
puissance oprératoire de cette physique est considérable.
Elle est désormais utilisée par les physiciens nucléaires
et atomistes, par les physiciens du solide et même par les astrophysiciens.
A ce jour, aucune expérience n'est venue démentir ses prédictions,
aussi étranges soient-elles. La physique quantique utilisant des
concepts qui n'ont pas toujours de contrepartie dans la vie courante, il
ne faut pas s'étonner si certaines de ses prédictions heurtent
si violemment le sens commun.
Albert Einstein, pour ne citer que lui, n'a jamais accepté
certaines des conséquences de la théorie quantique: voyez
comme il lui tire la langue!
![]()
![]() Pourquoi
le mot "quantique"?
Pourquoi
le mot "quantique"?
 La
physique quantique signifie littéralement "physique des quanta"
(= pluriel latin de "quantum" qui signifie quantité).
La
physique quantique signifie littéralement "physique des quanta"
(= pluriel latin de "quantum" qui signifie quantité).
Ce nouveau mot apparaît dans le registre de la physique le 14
Décembre 1900 grâce à un mémoire révolutionnaire
lu devant l'Académie des sciences de Prusse par l'Allemand Max
Planck: Ce dernier postule l'idée originale selon laquelle les
échanges d'énergie entre la lumière et la matière
ne peuvent se faire que par paquets discontinus, que l'on appellera les
quanta. Il renonce ainsi à la loi sacrée de la continuité,
pilier de la physique classique.
![]()
![]() Qu'est
ce que la lumière "classique" et continue ?
Qu'est
ce que la lumière "classique" et continue ?
 Pas si
facile de se représenter un tel concept immatériel!
Pas si
facile de se représenter un tel concept immatériel!
A la fin du XIXe siècle, James
Maxwell définit la lumière comme étant un faisceau
d'ondes électromagnétiques se déplaçant
à vitesse constante dans le vide: la fameuse vitesse c de
300.000 kilomètres par seconde.
Autant il est aisé de s'imaginer une onde parcourant la surface
de l'eau et le son comme étant une vibration de l'air, autant le
concept d'onde électromagnétique (comme étant une
oscillation de champs électrique et magnétique associés)
a de quoi laisser perplexe. Comment imaginer ces champs intimement liés?
quel est le support de cette oscillation dans le vide?
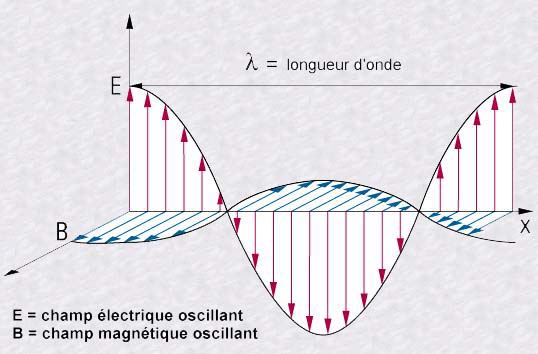
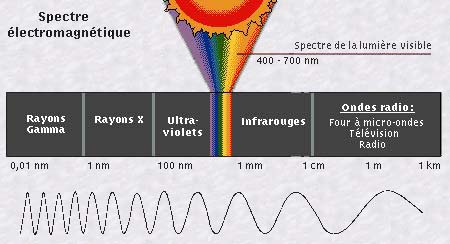
Toujours est-il que la lumière est caractérisée
par sa fréquence ou sa longueur d'onde. La lumière
n'est donc qu'une fenêtre étroite de l'ensemble des ondes
électromagnétiques (qui comprennent aussi les rayons gamma,
X, ultraviolets, infrarouges, les ondes radios...). Voir spectre)
![]()
![]() La
lumière photonique et quantique
La
lumière photonique et quantique
 Après
Max Planck, cette notion radicalement nouvelle de "lumière quantique"
sera reprise en 1905 par Albert Einstein qui soutiendra que l'énergie
de la lumière est en quelque sorte "granuleuse". Ce "grain d'énergie"
sera appelé photon en 1926. Une nouvelle particule est née,
particule immatérielle et sans masse.
Après
Max Planck, cette notion radicalement nouvelle de "lumière quantique"
sera reprise en 1905 par Albert Einstein qui soutiendra que l'énergie
de la lumière est en quelque sorte "granuleuse". Ce "grain d'énergie"
sera appelé photon en 1926. Une nouvelle particule est née,
particule immatérielle et sans masse.
Chaque photon d'un rayonnement (lumière, ondes radios, rayons
X...) est porteur d'un quantum d'énergie caractéristique
de sa fréquence (fréquence de la lumière = couleur).
La physique quantique va donc associer une onde et une particule. Cette
association se généralisera d'ailleurs a toute particule,
et notamment l'électron.
Mais comment concilier du continu (ondes) avec du discontinu (particules)?
C'est tout le paradoxe de la dualité onde-corpuscule
![]()
![]() La
dualité onde-corpuscule
La
dualité onde-corpuscule
La remise en cause la plus importante à laquelle oblige la physique quantique concerne la manière de représenter les objets physiques et leurs propriétés. L'ancienne physique, dite classique, distingue deux sortes d'entités fondamentales:
La physique quantique ne retient pas cette classification pourtant
bien commode. Les objets qu'elle considère ne sont ni des corpuscules,
ni des ondes, mais "autre chose".
Aidons-nous
de l'analogie suivante:
Regardé sous deux angles différents, un cylindre nous
apparaît tantôt comme un cercle, tantôt comme un rectangle.
Pourtant il n'est ni l'un ni l'autre.
Ainsi en est-il du photon, de l'électron ou de toute particule
élémentaire dont l'image corpusculaire ne serait qu'une facette
d'une entité plus complexe.
Ce point précis peut poser un problème philosophique très
troublant: La réalité objective (s'il elle existe indépendemment
de l'esprit humain) est-elle accessible ? Ou sommes-nous condamner à
n'observer qu'un monde d'appararences trompeuses?
![]()
![]() D'où
vient la lumière?
D'où
vient la lumière?
La physique quantique permet de mieux comprendre comment la lumière
est émise par la matière...
Le modèle de l'atome de Niels Bohr était un modèle
à la frontière de deux âge: l'âge classique pré-quantique
et le monde quantique. Mais il expliquait déjà le mécanisme
de l'émission de lumière par un atome
: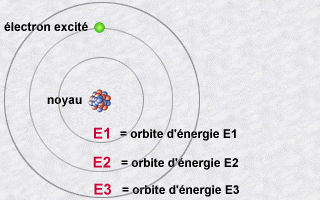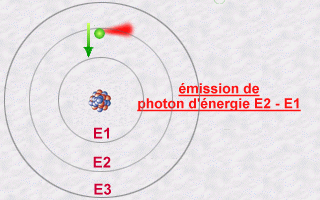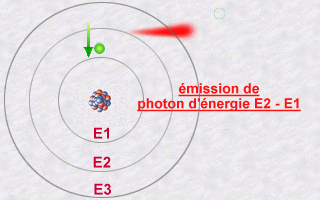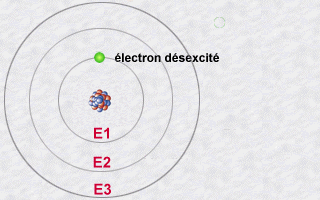
Cette émission s'explique alors par le saut qu'effectue un électron
d'une orbite E2 à une orbite E1. Pendant ce saut vers l'orbite E1
moins énergétique (une orbite plus intérieure), l'électron
va céder une partie de son énergie sous forme d'un photon
émis vers l'extérieur.
L'énergie de ce photon, E2 - E1, sera un multiple entier (la fameuse quantification de la lumière) de la valeur hn.
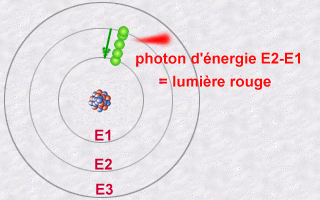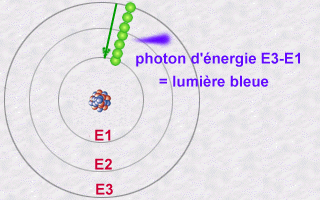
Inversement,
l'électron d'un atome pourra absorber un photon d'énergie
donnée en ainsi sauter d'une orbite peu énergétique
à une orbite plus énergétique: Il sera ainsi excité
car sur une orbite plus énergétique que la normale. C'est
en se désexcitant qu'il pourra réémettre un photon.
<------Cliquez sur
le dessin pour l'agrandir!
La théorie
quantique stipule que toutes les orbites électroniques ne sont pas
autorisées. Ces orbites ne sont permises que dans la mesure où
un électron, sautant d'une orbite à une autre, peut émettre
ou absorber un photon d'une énergie multiple de la fameuse valeur
hn.
C'est cette discontinuité quantique de l'énergie échangée
qui entraîne une discontinuité des orbites permises. Chaque
orbite électronique autorisée sera donc quantifiée
et caractérisée par des nombres quantiques (4 nombres
notés n, l, m et s).
Par exemple, le nombre n s'appelle le nombre quantique principal.
Il désigne le numéro de la couche électronique aussi
désignée par les lettres K, L, M, O, P, Q.
![]()
Chaque atome ne peut donc émettre qu'une palette précise
de couleurs caractéristiques : Chaque couleur de la lumière
est en fait une fréquence particulière (et donc un niveau
d'énergie) de photon. Tous les sauts d'électrons entre toutes
les orbites possibles au sein d'un même atome se traduisent donc
par l'émission (ou l'absorbtion) d'un spectre de lumière
caractéristique: Il s'agit là d'une véritable carte
d'identité d'un type d'atome donné. C'est grâce à
ce spectre facilement identifiable que l'on peut savoir quels atomes existent
dans les étoiles du firmament. Leur lumière est captée
par les télescopes, analysée et comparée avec les
spectres de l'hydrogène, de l'hélium etc...